Пятилетнему пациенту после генной терапии удалили опухоль мозга
В США у пятилетнего мальчика, лечившегося от редкого наследственного заболевания с помощью генной терапии, спустя около четырёх лет обнаружили нейроэпителиальную опухоль мозга, которую удалось полностью удалить. Исследование в New England Journal of Medicine указывает на встраивание фрагментов вирусного вектора в ген, связанный с ростом опухолей, но прямая причинно‑следственная связь пока не доказана.
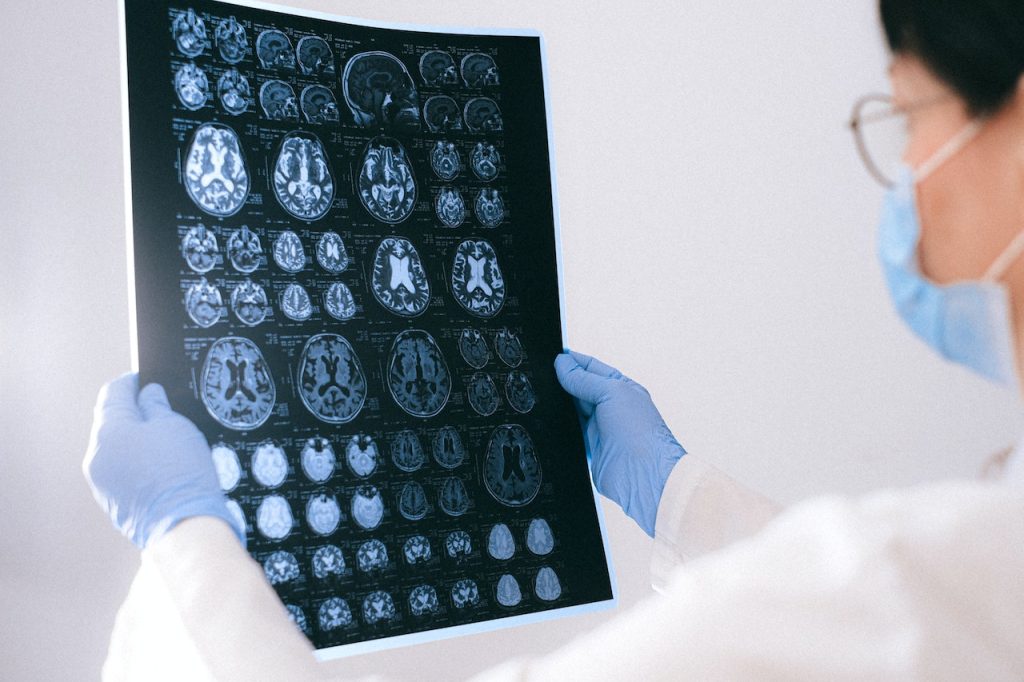
Ключевые факты
- Пациент: 5 лет, лечится в Детской больнице Филадельфии; ранее получил генную терапию против мукополисахаридоза I типа (MPS I).
- Диагноз при рождении: тяжёлая форма MPS I из‑за мутации в гене IDUA; без лечения дети редко доживают до подросткового возраста.
- Лечение: препарат RGX‑111 — аденоассоциированный вирус (AAV) доставил рабочую копию гена IDUA.
- Через ~4 года: обнаружена нейроэпителиальная опухоль мозга; опухоль полностью удалили хирургически.
- Исследование: опубликовано в New England Journal of Medicine; в опухолевой ткани нашли фрагменты вирусного материала, встроившиеся рядом с геном PLAG1, который ассоциирован с опухолевым ростом.
- Оценка риска: учёные рассматривают встраивание как возможный фактор, но прямых доказательств причинно‑следственной связи недостаточно; такие случаи остаются крайне редкими.
- Регуляция: FDA ранее ограничивало клинические испытания RGX‑111 и RGX‑121; часть ограничений затем сняли. Другие генные терапии (например, Zolgensma) продолжают применяться — подтверждённой связи с раком у них не показано.
Что такое MPS I и почему нужна генная терапия
Мукополисахаридоз I (MPS I) — редкое наследственное заболевание, вызванное дефектом гена IDUA, из‑за которого нарушается расщепление сложных углеводов (гликозаминогликанов). Накопление этих веществ приводит к поражению внутренних органов, костно‑суставной системы и нервной ткани. Тяжёлые формы болезни часто сокращают продолжительность жизни, потому ранняя и эффективная терапия критична. Традиционные подходы включают заместительную ферментную терапию и пересадку стволовых клеток, но они имеют ограничения в воздействии на нервную систему.
Как работает RGX‑111 и AAV‑векторы
RGX‑111 использует рекомбинантный аденоассоциированный вирус (AAV) как «курьера» для доставки здравого варианта гена IDUA в клетки пациента. AAV обычно считается относительно безопасным в клинической практике: он редко интегрируется в геном хозяина и чаще сохраняется в эпизодической (неинтегрированной) форме. Тем не менее в редких случаях фрагменты вектора могут встроиться рядом с генами хозяина и потенциально повлиять на их активность.
Что нашли учёные в этом случае
Патологоанатомический анализ удалённой опухоли показал присутствие фрагментов вирусного материала рядом с геном PLAG1, известным как онкогенный фактор при некоторых опухолях. Авторы отмечают, что такое событие может способствовать опухолеобразованию, но единственного случая недостаточно, чтобы утверждать прямую причинно‑следственную связь. Требуются дополнительные наблюдения, большие когорты пациентов и молекулярные исследования, чтобы оценить частоту и механизм риска.
Регуляторные и клинические последствия
После сообщений о возможных рисках FDA ввело ограничения на некоторые испытания RGX‑111 и RGX‑121; позже часть ограничений сняли по мере накопления данных. Эксперты подчёркивают: преимущества генной терапии для тяжёлово больных пациентов могут перевешивать редкий риск, но необходимы усиленный мониторинг, тщательная молекулярная проверка опухолевых образцов и долгосрочные регистры пациентов. Другие векторы и препараты продолжают использоваться, и на сегодняшний день у них нет подтверждённой связи с повышенной частотой злокачественных опухолей.
Что это значит для пациентов и врачей
- Пациенты и семьи: случаи, подобные этому, требуют прозрачного информирования о потенциальных рисках и долгосрочном наблюдении после терапии. Решение о применении генной терапии должно взвешивать тяжесть исходного заболевания и доступные альтернативы.
- Для клинических исследований: важно внедрять стандарты мониторинга интеграции вектора, хранить биобанки образцов и проводить молекулярный анализ при появлении новообразований.
- Для регуляторов: баланс между доступом к инновациям и контролем безопасности остаётся ключевым — нужны обновлённые руководства и критерии оценки риска интеграции векторов.
Ранее мы писали, что женщина стала инвалидом из-за врачей, нажавших не на ту кнопку.